人民网上海1月15日电 1月11日,由中国医药生物技术协会和《中国医药生物技术》杂志共同主办的“2019年中国医药生物技术十大进展评选”活动落下帷幕。


上海细胞治疗集团总裁、国家杰出青年科学基金获得者、国家重点研发计划项目精准医疗专项首席科学家钱其军教授团队研发的非病毒载体制备的CAR-T细胞治疗产品BZ019,从20个候选项目中脱颖而出,摘获该年度“中国医药生物技术十大进展”,也是本年度“中国医药生物技术十大进展”中唯一上榜CAR-T细胞治疗技术。据介绍,该产品获得国家药品监督管理局许可开展临床试验,用于CD19阳性成人复发或难治性弥漫大B细胞淋巴瘤,这是目前国内第一家也是唯一一家进入临床试验的非病毒载体制备CAR-T细胞治疗产品。
行行查,行业研究数据库: www.hanghangcha.com
CAR-T本质上是一种T淋巴细胞,与人体普通的T细胞相似,区别在于科学家通过基因工程的方法向T细胞导入了一段人工改造的DNA,使T细胞能利用这段DNA表达“CAR”这个融合蛋白,从而产生了识别特定肿瘤细胞的能力,再结合T细胞自身携带的杀伤肿瘤细胞的功能,达到CAR-T在人体组织中找出肿瘤细胞并将其消灭、治疗肿瘤的目的。

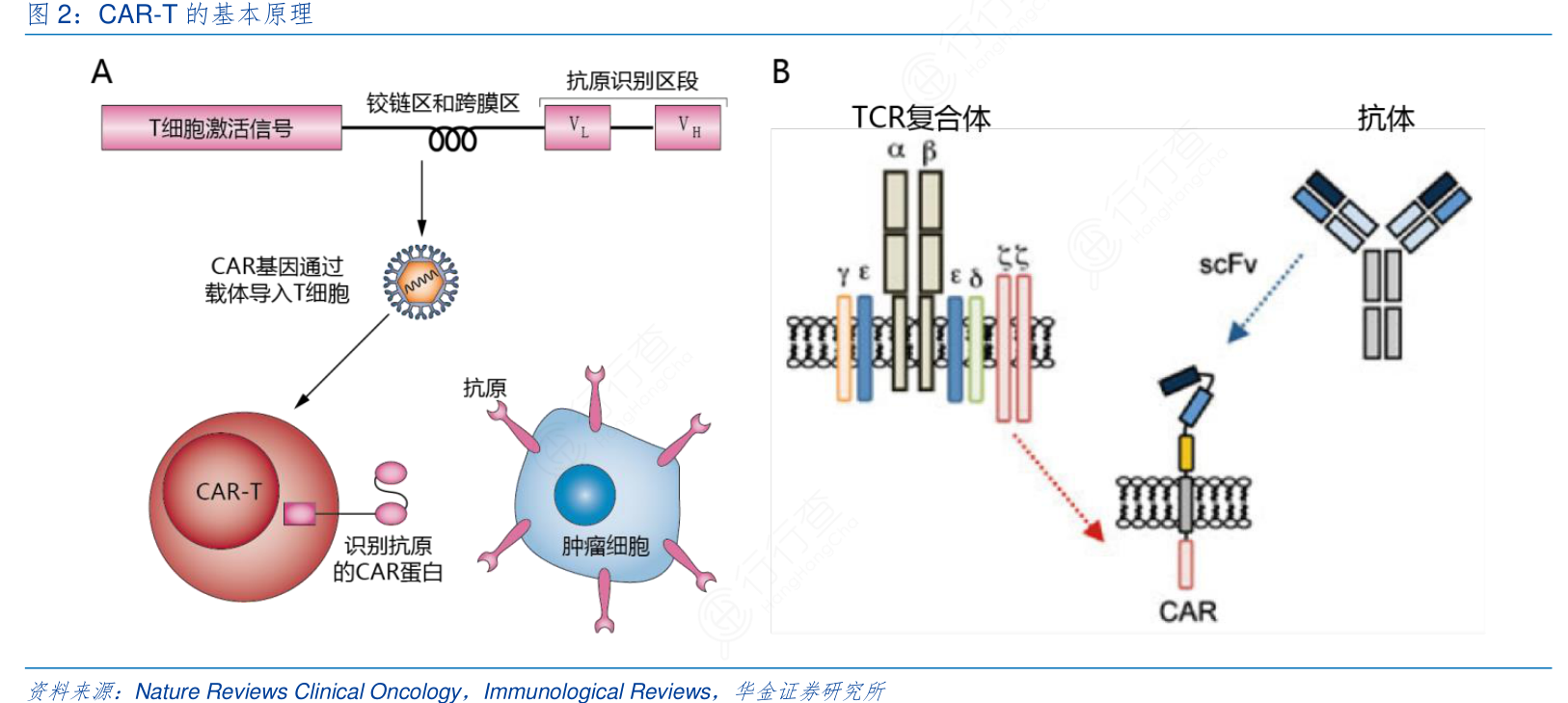
CAR-T治疗的过程可分为“捕获”、“改造”、“回输”三个步骤。(1)T细胞的捕获:收集患者的外周血,再经过纯化分离,最终获得患者自体来源的T细胞。(2)T细胞基因改造:这个过程耗时约10天,利用病毒载体等方式将CAR基因导入T细胞,使其获得识别肿瘤和增殖的能力,再对CAR-T进行扩增,达到治疗所需要的细胞数量。(3)化疗:在对T细胞进行基因改造的同时,部分临床方案会对病人进行化疗等辅助治疗,让病人本身的淋巴细胞耗竭,以加强CAR-T的治疗效果。虽然部分临床试验结果发现耗竭淋巴细胞有利于CAR-T治疗,但尚未最终定论。(4)T细胞回输:将扩增好的CAR-T回输到病人体内,同时对病人的生理反应进行监测。


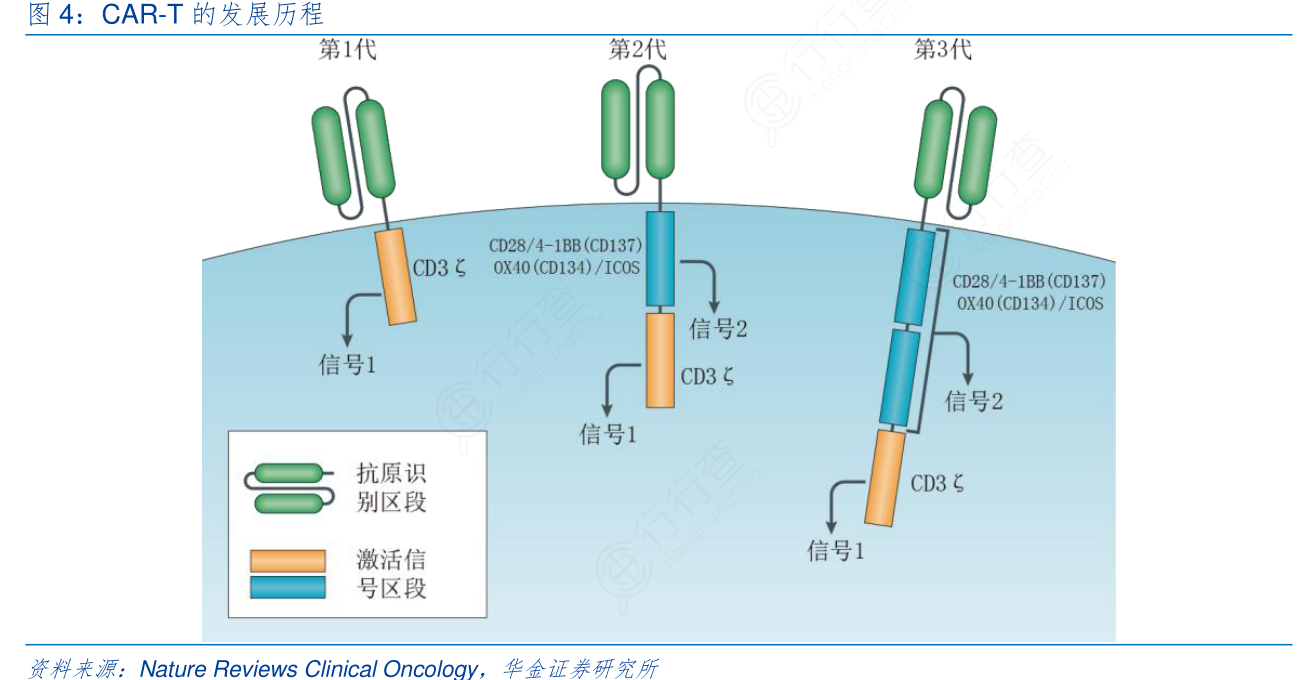
截至目前,CAR-T已经经历了三代的发展,主要体现在CAR结构的改造上。(1)第一代CAR-T的CAR结构相对简单,激活信号区段仅含CD3δ,其临床表现并不理想,推测由于激活信号不够强引起CAR-T在病人体内缺乏长期增殖能力以及激活引起的细胞自身凋亡所致。(2)第二代CAR-T依然沿用了上一代CAR-T的基本骨架,只是在CD3δ前端另外加了一个共刺激信号,基本解决了CAR-T增殖受限的问题。目前用得最多的共刺激信号是CD28或4-1BB,二者在临床上没有表现出显著的区别。(3)第三代CAR-T在第一代的基础上加了两个共刺激信号,用的比较多的是CD28/4-1BB和CD28/OX40(CD134)组合。第三代CAR-T是否比第二代CAR-T有明确优势目前尚未定论。(4)“准四代”CAR-T于近年开始出现,在第二代CAR-T的基础上进行改造,使CAR-T具有额外的功能,如共表达PD1单抗等,加强CAR-T的肿瘤杀伤效果。但目前“准四代”CAR-T存在多个版本,且其功效还未得到严格地论证,因此也不存在和前三代CAR-T一样公认的第四代CAR-T技术。

行行查,行业研究数据库: www.hanghangcha.com
手机访问“行行查”小程序更方便
![]()

![]()

![]()

![]()

![]()

![]()

![]()

![]()

![]()

![]()

![]()

![]()
